À medida que mais pessoas com diabetes tipo 2 (T2D) tomam medicação para controlar os níveis de açúcar no sangue e perder peso, têm surgido preocupações sobre a sua segurança. A evidência do mundo real da base de dados do Sistema de Notificação de Eventos Adversos (FAERS) da Administração de Alimentos e Medicamentos dos EUA mostra agora um perfil de segurança tranquilizador para o tirzepatide (TZP).
O triazepatide, agonista duplo do polipeptídeo insulinotrópico dependente da glicose (GIP)/recetor do péptido semelhante ao glucagon 1 (GLP1), demonstrou uma elevada eficácia na redução dos níveis de glicose no sangue e do peso corporal em pessoas com diabetes tipo 2 e/ou obesidade. Os agonistas dos receptores GLP1 reduzem o apetite e retardam o esvaziamento gástrico, pelo que são cada vez mais utilizados no tratamento da obesidade.
Ensaios clínicos aleatorizados mostraram que o perfil de segurança da TZP é semelhante ao de outros antirretrovirais GLP1 e caracteriza-se principalmente por acontecimentos gastrointestinais adversos. No entanto, foram levantadas preocupações sobre uma possível associação entre a TZP e a retinopatia diabética, as perturbações pancreatobiliares e o cancro medular da tiroide, mas ainda não foram apresentadas provas claras.
Para saber mais, a Dra. Irene Caruso do Departamento de Medicina Interna, Endocrinologia, Andrologia e Doenças Metabólicas da Universidade de Bari, Itália, e os seus colegas pesquisaram a base de dados de vigilância pós-comercialização FAERS, que contém relatórios de fabricantes, doentes e profissionais de saúde. Pretendiam descobrir se surgiram preocupações de segurança semelhantes na experiência do mundo real [1].
Os investigadores recuperaram relatórios de eventos adversos relacionados com a TZP que estavam associados a perturbações gastrointestinais, pancreatite, colecistite e colelitíase, retinopatia diabética e neoplasias da tiroide. Foi calculado um rácio de probabilidades de notificação (ROR) para avaliar a desproporcionalidade da notificação de determinados acontecimentos adversos associados à TZP em comparação com outros medicamentos. A análise foi então filtrada por relatos de idade, sexo e o medicamento designado como principal suspeito. A ocorrência de acontecimentos adversos com a TZP foi também comparada separadamente com outros tratamentos para a diabetes, incluindo a insulina, os inibidores SGLT2, a metformina e os GLP1-RA (tanto individualmente como enquanto classe).
De um total de 20 409 relatórios sobre 1432 acontecimentos adversos, os investigadores analisaram 7460 relatórios relativos a 286 acontecimentos adversos selecionados (cancro do trato gastrointestinal, do pâncreas, da vesícula biliar, dos olhos e da tiroide), 22 dos quais revelaram um sinal de desproporcionalidade.
Menor risco de náuseas, mas maior risco de obstipação
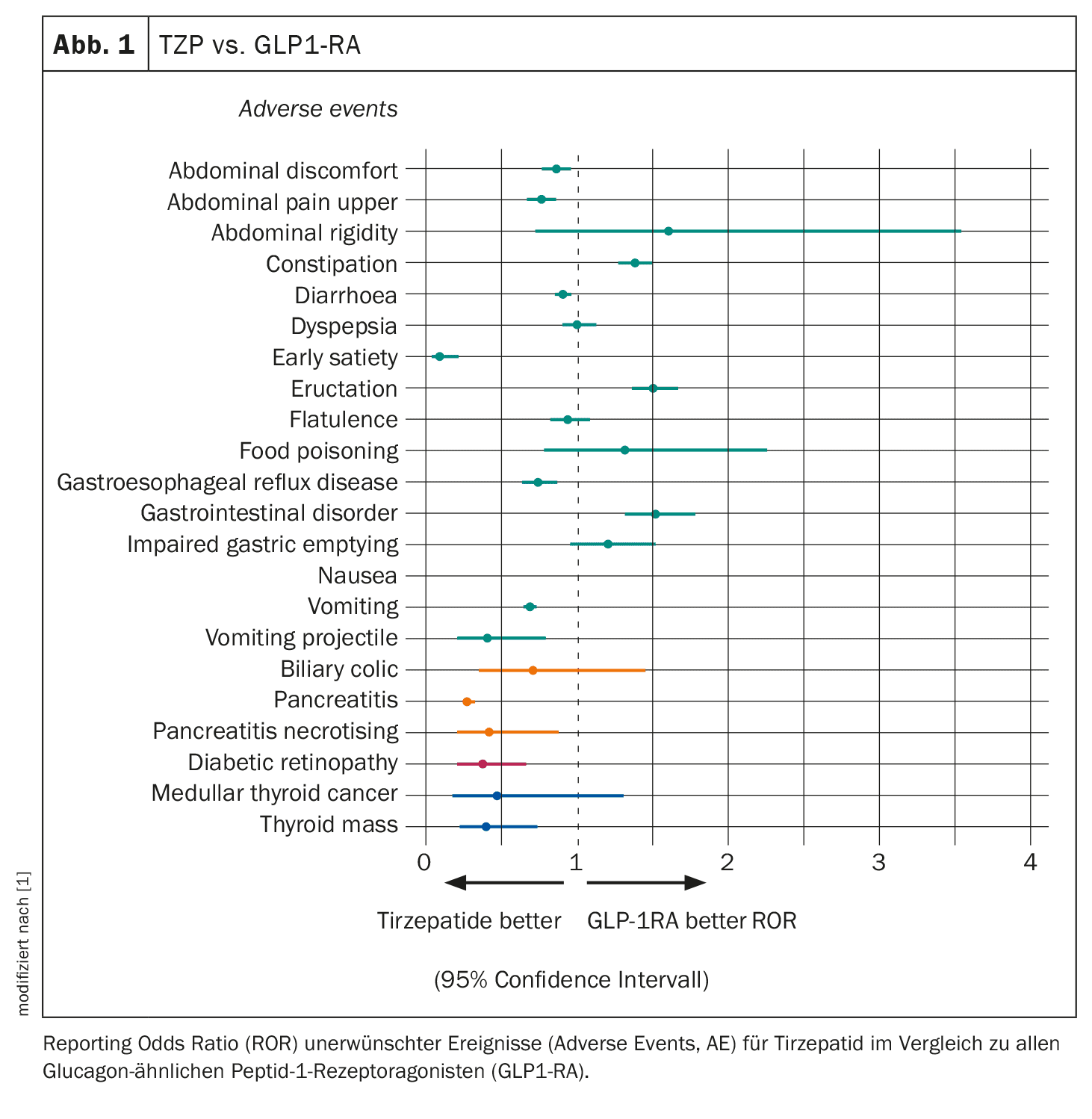
Os relatos de regurgitação foram 30 vezes mais prováveis com TZP do que com outros medicamentos, enquanto náuseas, dispepsia, obstipação e pancreatite foram quatro vezes mais prováveis com TZP do que com todos os outros medicamentos. No entanto, a TZP foi associada a um risco de acontecimentos adversos gastrointestinais semelhante ao dos outros GLP-1RA, com algumas diferenças, incluindo um menor risco de náuseas e um maior risco de obstipação (Fig. 1). Como esperado, a TZP apresentou um risco mais elevado da maioria dos eventos adversos gastrointestinais em comparação com a insulina e os inibidores SGLT2. Não foi observada uma notificação desproporcionada de pancreatite com a TZP em comparação com os SGLT2i, mas foi descrito um risco mais elevado em comparação com a insulina e um risco mais baixo em comparação com os GLP1-RA.
Os investigadores descobriram também uma incidência desproporcionadamente elevada de cancro medular da tiroide com a TZP, com uma probabilidade 13 vezes superior em comparação com todos os outros medicamentos (com base em três eventos). No entanto, a TZP foi associada a um risco de cancro medular da tiroide semelhante ao de outros inibidores GLP1-RA e SGLT2 e a um risco mais elevado em comparação com a insulina.
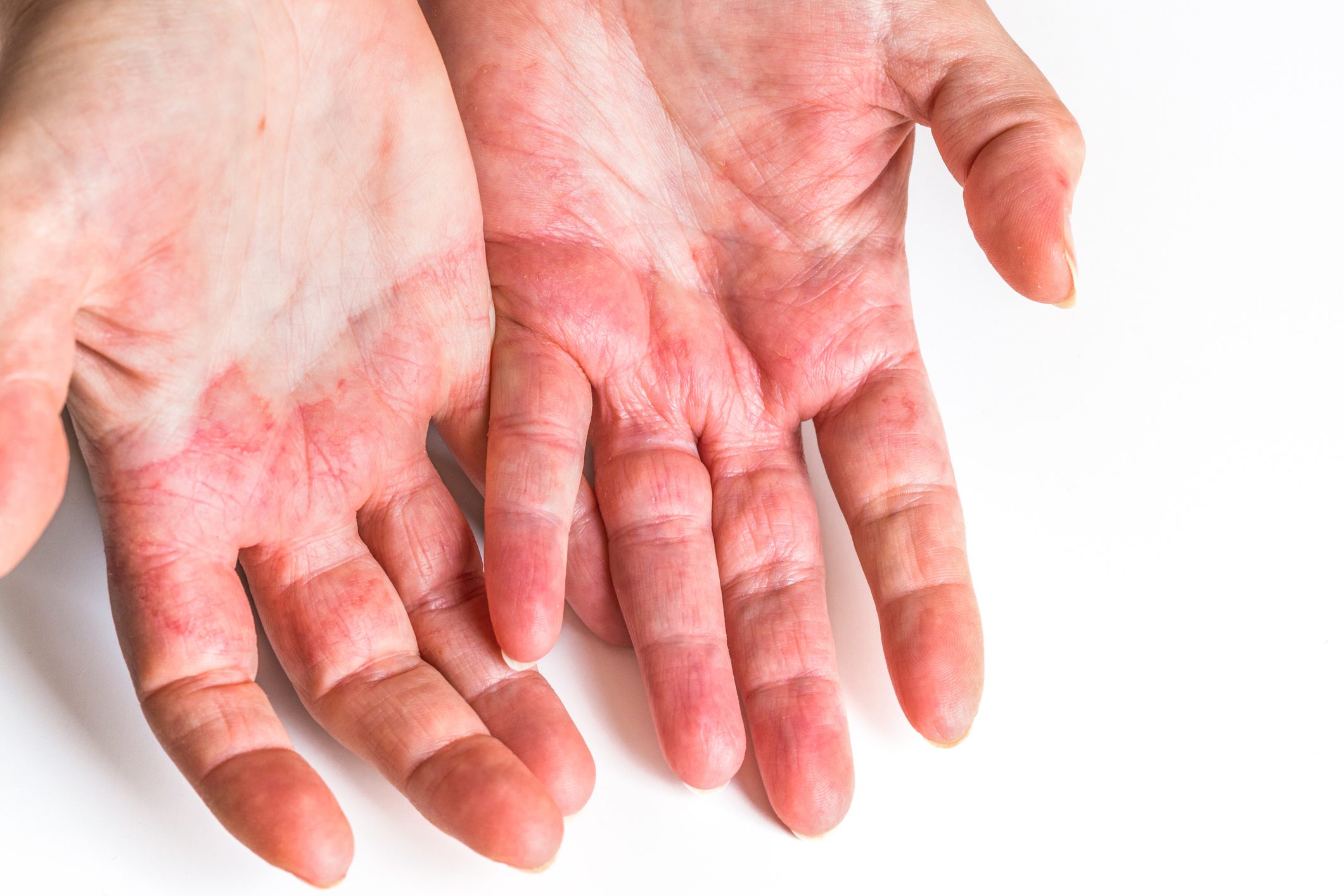
Da mesma forma, a TZP tinha mais de três vezes mais probabilidades de causar retinopatia diabética (com base em 12 casos) do que qualquer outro medicamento. No entanto, o medicamento apresentou um risco semelhante ao dos inibidores SGLT2 e um risco consistentemente inferior ao dos GLP1-RA e da insulina. Não foi observado um número desproporcionado de acontecimentos adversos relacionados com a vesícula biliar e as vias biliares, com exceção de um risco aumentado de cólica biliar em comparação com todos os outros medicamentos e a insulina. Em comparação com o GLP1-RA e o SGLT2i, o risco de cólica biliar foi comparável.
Estes resultados mostraram que a tirzepatide tem uma tolerabilidade gastrointestinal (GI) semelhante à da classe dos GLP1-RA, sem um risco acrescido de pancreatite, retinopatia diabética e cancro medular da tiroide, concluiu o Dr. Caruso. O perfil de segurança da tirzepatide é, portanto, tranquilizador, embora com limitações.
Fonte: Caruso I: O perfil de segurança do tirzepatide no mundo real: análise de farmacovigilância da base de dados do Sistema de Notificação de Eventos Adversos da FDA (FAERS). Apresentação Oral #753, Sessão SO 063: Mais combo’s menos insulina! EASD, 11/09/2024.
Literatura:
- Caruso I, et al: O perfil de segurança do tirzepatide no mundo real: análise de farmacovigilância da base de dados do Sistema de Notificação de Eventos Adversos da FDA (FAERS). J Endocrinol Invest 2024; 47: 2671-2678; doi: 10.1007/s40618-024-02441-z.
InFo DIABETOLOGIE & ENDOKRINOLOGIE 2024; 1(4): 18–20 (publicado em 29.11.24, antes da impressão)
HAUSARZT PRAXIS 2024; 19(12): 50–51