Pulmonale Hypertonie ist in der Regel ein Zeichen für eine fortgeschrittene Linksherzerkrankung (PH-LHD). Das zentrale Merkmal der PH-LHD ist ein erhöhter pulmonal-arterieller Keildruck von >15 mmHg. In besonders ausgewählten Fällen kann eine für die pulmonale arterielle Hypertonie zugelassene Therapie, d.h. Phosphodiesterase-5-Inhibitoren (PDE5i), als Überbrückung bis zur Herztransplantation und nach einem linksventrikulären Unterstützungssystem im Falle einer stark eingeschränkten rechtsventrikulären Funktion angezeigt sein. Bei mittelschwerer bis schwerer Mitralinsuffizienz sollten die Behandlungsoptionen (chirurgische oder Transkatheter-Klappenreparatur) in einem Herzteam aus Kardiologen, Herzchirurgen und Bildgebungsspezialisten geprüft werden.
Pulmonale Hypertonie (PH) kann die Folge aller Ursachen einer Linksherzerkrankung (LHD) sein und ist in der Regel ein Zeichen für ein fortgeschrittenes Stadium der LHD (Tabelle 1). Die fortschreitenden Symptome der Herzinsuffizienz mit Belastungsintoleranz aufgrund von PH-LHD führen nachweislich zu einem schlechteren Ergebnis, je nachdem, wie früh und effektiv die LHD behandelt werden kann [1].

Definition von PH-LHD
PH wird im Allgemeinen für alle klinischen Gruppen als ein hämodynamischer und pathophysiologischer Zustand mit einem erhöhten mittleren pulmonal-arteriellen Druck (PAPm) in Ruhe von ≥25 mmHg definiert, der durch eine Rechtsherzkatheteruntersuchung ermittelt wird. Das zentrale Merkmal der PH-LHD ist ein erhöhter pulmonal-arterieller Keildruck (PAWP) von >15 mmHg, der auf einen erhöhten Füllungsdruck des linken Atriums und eine postkapilläre PH zurückzuführen ist.
Die Leitlinien der Europäischen Gesellschaft für Kardiologie und der European Respiratory Society (ESC/ERS) von 2009 für die Diagnose und Behandlung der PH definieren die hämodynamischen Merkmale der PH-LHD anhand des transpulmonalen Gradienten (TPG), der Differenz zwischen PAPm und PAWP [1,2]. Die postkapilläre PH-LHD wird entweder als passiv (TPG ≤12 mmHg) oder reaktiv (unverhältnismäßig, TPG >12 mmHg) definiert. In 10-15% der Fälle weist die Hämodynamik auf eine Kombination aus prä- und postkapillarer PH hin [1]. Die alleinige Berücksichtigung des TPG kann jedoch zu einer Fehlklassifizierung der PH-LHD führen, was sich auf den therapeutischen Ansatz der LHD auswirkt.
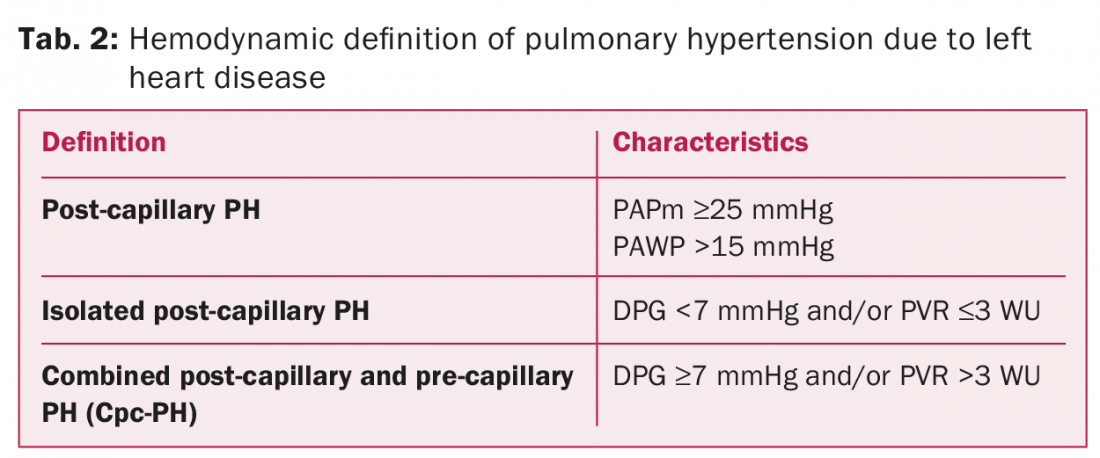
Die PH-Leitlinien 2015 von ESC/ESR definieren drei verschiedene hämodynamische Zustände bei der Interpretation der PH-LHD (Tabelle 2) [3]. Die wichtigsten Änderungen in den Merkmalen der PH ist die Auswertung des diastolischen Druckgradienten (DPG), der Differenz zwischen PAPd und PAWP anstelle des TPG und/oder des peripheren Gefäßwiderstands, um eine isolierte postkapilläre PH (Ipc-PH) von einer kombinierten post- und präkapillären PH (Cpc-PH) zu unterscheiden (Tabelle 2).
Patienten, die einen pulmonalen Gefäßwiderstand (PVR) von mehr als fünf Wood-Einheiten (5 WU×80 = 400 dyn×sec×m2×cm-5) oder einen PVR-Index >6 WU haben, haben ein erhöhtes Risiko einer postoperativen rechtsventrikulären Insuffizienz nach einer Herztransplantation [4]. Daher sind pharmakologische “vasodilatatorische Herausforderungen” entweder direkt auf das pulmonal-arterielle Gefäßsystem gerichtet, wie z.B. Prostazyklin, oder im Falle einer unzureichenden Reaktion, d.h. bei sehr hohem PAWP, eine Nachlastsenkung am linken Herzen mit Nitroprussid oder Nitroglyzerin notwendig, um die irreversibel “fixierte” pulmonal-arterielle Hypertonie (PAH) zu demaskieren.
Bei Patienten mit fixiertem, erhöhtem peripheren Gefäßwiderstand kann eine begleitende Lungenerkrankung, obstruktive Schlafapnoe oder eine chronische pulmonale thromboembolische Erkrankung vorliegen, die bei der Differentialdiagnose berücksichtigt und ausgeschlossen werden sollte.
Medizinische Behandlung
Für die medikamentöse Behandlung von PAH gibt es gesicherte und wachsende Erkenntnisse, während für PH-LHD keine Daten vorliegen. Medikamente, die sich bei PAH als wirksam erwiesen haben, werden jedoch zunehmend auch bei anderen Formen der PH einschließlich PH-LHD eingesetzt, z. B. Phosphodiesterase-5-Inhibitoren (PDE5i).
Man nimmt an, dass die positiven Wirkungen von PDE5i bei PAH auf relativ selektive gefäßerweiternde und antiproliferative Wirkungen auf das pulmonale Gefäßsystem sowie auf die Hämodynamik bei Herzinsuffizienz zurückzuführen sind [5]. Die PH ist der wichtigste pathophysiologische Mechanismus bei rechtsventrikulärem Versagen [4]. Kleine Studien bei Patienten mit Herzinsuffizienz zeigten den größten Nutzen von PDE5is bei Patienten mit PH-LHD und rechtsventrikulärer Insuffizienz [5]. Man nimmt an, dass dies auf die direkte Wirkung von PDE5i auf die rechtsventrikuläre Myokardkontraktilität zurückzuführen ist, da die PDE5-Expression in geschädigten rechten Herzkammern nachweislich hochreguliert ist [6]. Die PDE5-Hemmung kann daher eine Rolle bei der Verbesserung der rechtsventrikulären Funktion bei Herzinsuffizienz spielen und könnte bei einigen sorgfältig ausgewählten Patienten als Überbrückung bis zur Herztransplantation oder nach einer Unterstützung durch ein linksventrikuläres Hilfsgerät klinisch gerechtfertigt sein. Dies wird im ersten Fallbericht erörtert.
Fall 1: Ein junger Patient mit dilatativer Kardiomyopathie
46-jähriger Patient mit bekannter dilatativer Kardiomyopathie seit dem Jahr 2000 und einer linksventrikulären Auswurffraktion (LVEF) von 20%, normaler rechtsventrikulärer Größe und Funktion, leichter Mitralinsuffizienz und fehlender PH bei der Rechtsherzkatheteruntersuchung (Abb. 1).
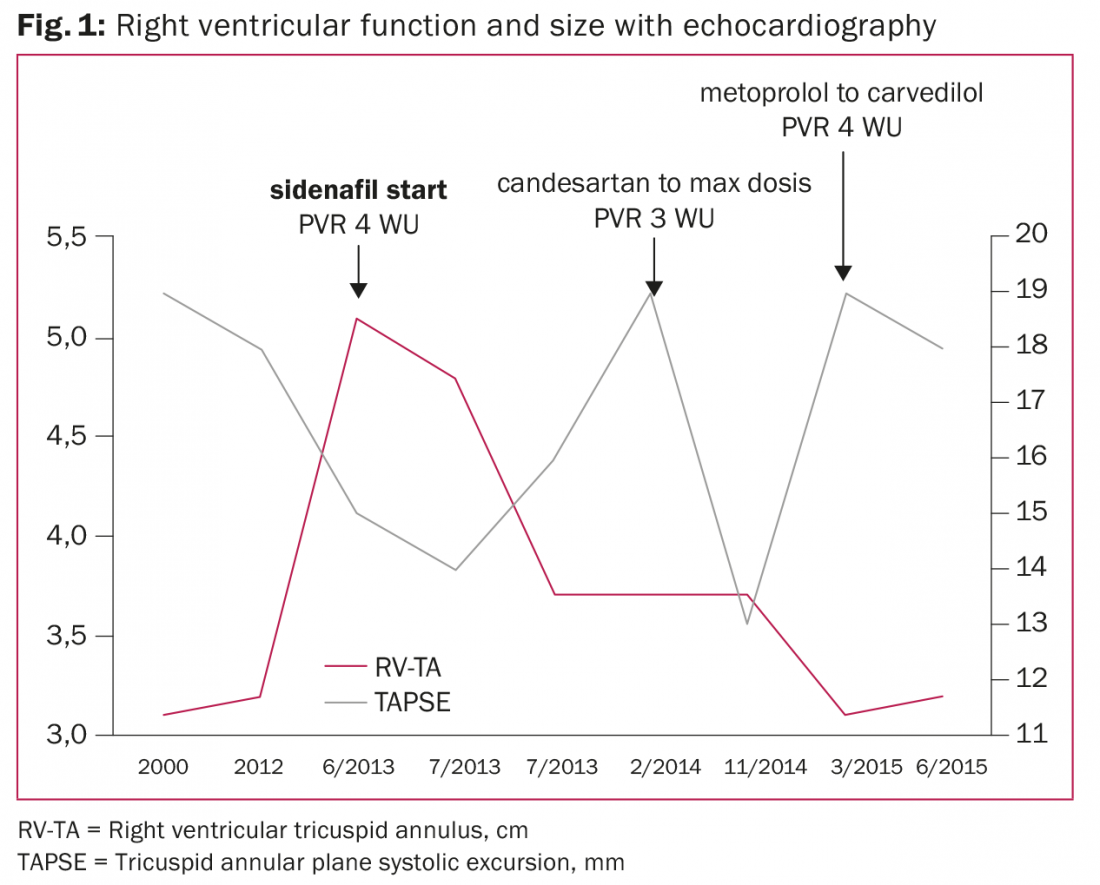
Im Jahr 2012 wurde ihm aufgrund einer Synkope und eines erneuten Linksschenkelblocks eine kardiale Resynchronisationstherapie mit Defibrillator implantiert. Im Jahr 2013 wurde der Patient aufgrund einer akuten biventrikulären Herzdekompensation, eines dilatierten rechten Ventrikels und einer eingeschränkten rechtsventrikulären Funktion zur Untersuchung an das Herzinsuffizienzteam überwiesen. Der TPG betrug 12 mmHg, aber der DPG lag bei -1 mmHg, was auf eine isolierte postkapilläre PH und eine PVR von 4,4 WU (352 dyn×sec×m2×cm-5) nach dem Ilomedin-Vasodilatationstest hinweist. Es wurde kein pharmakologischer Test zur systemischen Vasodilatation (d. h. Nitroprussid oder Nitroglyzerin) durchgeführt, um eine Cpc-PH oder irreversible PAH auszuschließen. Aufgrund der PH mit rechtsventrikulärem Versagen wurde daher eine Sildenafil-Therapie eingeleitet. Es wurde eine Untersuchung für eine Herztransplantation eingeleitet.
Es wurden serielle Rechtsherzkatheteruntersuchungen gemäß den Richtlinien der Internationalen Gesellschaft für Herz- und Lungentransplantation aus dem Jahr 2006 durchgeführt, um die Eignung für eine Herztransplantation festzustellen, um das hohe Risiko einer rechtsventrikulären Insuffizienz und die Sterblichkeit nach einer Herztransplantation zu vermeiden [7]. Ein Anstieg der PVR wurde 2014 (5,7 WU bis auf 2,8 WU nach dem systemischen Vasodilatationstest) und 2015 (4,3 WU) festgestellt und danach sank die PVR auf 1,3 WU (104 dyn×sec×m2×cm-5) nach fortgesetzter Optimierung der Herzinsuffizienztherapie.
Schon bald nach Beginn der Sildenafil-Behandlung normalisierte sich die Größe des rechten Ventrikels und die rechtsventrikuläre Funktion verbesserte sich im Laufe von zwei Jahren, trotz einer zeitweiligen Progression der PH. Der Patient ist klinisch stabil in der NYHA-Klasse III mit moderater Mitralinsuffizienz und steht auf der Warteliste für eine Herztransplantation.
Therapeutische Optionen: Ausgerichtet auf die zugrunde liegende Pathologie
Wenn die medikamentöse und gerätetechnische Therapie nicht zu einer Senkung der PVR <3-5 WU führt und der Patient in der NYHA-Klasse III-IV verbleibt, kann bei akzeptabler rechtsventrikulärer Funktion [7,8] ein linksventrikuläres Unterstützungssystem in Betracht gezogen werden. Gemäß den Leitlinien zur mechanischen Kreislaufunterstützung (MCS) von 2013 kann PDE5i zur Behandlung der rechtsventrikulären Dysfunktion bei PH nach MCS in Betracht gezogen werden (Evidenzgrad IIb, C) [8]. Die therapeutischen Möglichkeiten der PH-LHD sollten sich an der zugrunde liegenden Pathologie der LHD orientieren. Durch die Weiterentwicklung der chirurgischen Klappenreparatur und die Einführung perkutaner interventioneller Techniken, vor allem der Transkatheter-Aortenklappenimplantation (TAVI) und der perkutanen Edge-to-Edge-Klappenreparatur, haben sich neue Erkenntnisse, Diagnosetechniken und therapeutische Möglichkeiten ergeben. Diese Veränderungen stehen hauptsächlich im Zusammenhang mit Aortenstenose und Mitralinsuffizienz.
Fall 2: Eine 44 Jahre alte Frau mit dilatativer Kardiomyopathie
Die 44-jährige Patientin hat eine dilatative Kardiomyopathie (nach Alkoholmissbrauch) seit dem Jahr 2010, LVEF 30%, normale rechtsventrikuläre Größe und mäßig eingeschränkte rechtsventrikuläre Funktion. PH bei der Rechtsherzkatheteruntersuchung (PAPm 33 mmHg) mit isolierter postkapillarer PH (DPG 4 mmHg). Die Mitralinsuffizienz war schwerwiegend (effektive Regurgitationsöffnungsfläche 54 mm2 [reference ≥40], Regurgitationsvolumen 66,1 ml/Schlag [reference ≥60], Umkehrung des pulmonalvenösen Flusses) mit Vergrößerung des enddiastolischen Durchmessers des linken Ventrikels (61 mm) und des linken Atriums (47 mm).
Die Klappe war morphologisch intakt und erfüllte somit die echokardiographischen Kriterien einer funktionellen Mitralinsuffizienz [9]. Eine Therapie der Herzinsuffizienz wurde eingeleitet und ein implantierbarer Kardioverter-Defibrillator (ICD) implantiert. Die Mitralinsuffizienz verbesserte sich auf einen mittleren Grad.
Ende 2011 wurde der Patient aufgrund eines akuten Lungenödems und wiederholter ICD-Schocks wegen nicht anhaltender ventrikulärer Tachykardie zur weiteren Untersuchung an das Team für Herzinsuffizienz überwiesen. Die Mitralinsuffizienz war schwerwiegend. Die erreichte pharmakologische Therapie war aufgrund der Hypotonie submaximal. Der Patient erhielt die Anweisung, den Alkoholkonsum einzustellen und sich an eine strikte Volumen-/Salzaufnahme zu halten. Wie in Abbildung 2 zu sehen ist , wurde der Patient im darauffolgenden Jahr 2012 viermal wegen einer LH-Dekompensation ins Krankenhaus eingeliefert, wobei er sich zwischendurch stabilisieren konnte, jedoch weiterhin eine schwere Mitralinsuffizienz aufwies. Aufgrund der schlechten Compliance war eine Herztransplantation oder eine Therapie mit einem linksventrikulären Hilfsgerät relativ kontraindiziert.
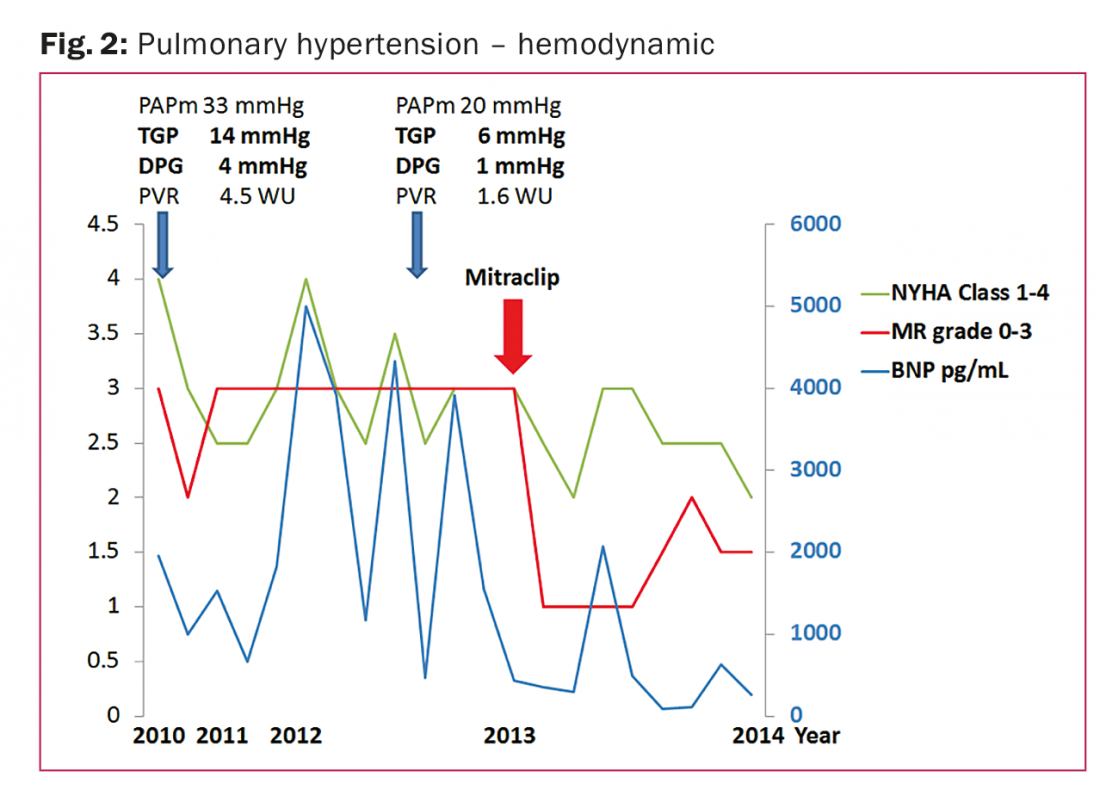
Im Jahr 2013 wurde eine perkutane Edge-to-Edge-Reparatur mit dem Mitraclip erfolgreich durchgeführt, wodurch die Mitralinsuffizienz sofort auf einen leichten Grad reduziert wurde. Im folgenden Jahr kam es zu keinen weiteren Krankenhausaufenthalten aufgrund einer LH-Dekompensation. Der Patient ist klinisch stabil in der NYHA-Klasse II, hat niedrige BNP-Werte und eine leichte Mitralregurgitation.
Behandlung der Mitralinsuffizienz
Die Echokardiographie ist die wichtigste Untersuchung zur Beurteilung der Mitralinsuffizienz und muss eine sorgfältige Beurteilung der Klappenanatomie, des Schweregrads der Mitralinsuffizienz, ihrer Mechanismen (d.h. funktionelle vs. degenerative Mitralinsuffizienz) und der Frage nach der Reparierbarkeit der Klappe umfassen. Die Folgen der Mitralinsuffizienz werden durch die Messung des Durchmessers des linken Atriums, des Durchmessers des linken Ventrikels, der LVEF und des systolischen pulmonal-arteriellen Drucks beurteilt. Die aktuellen ESC-Leitlinien für die Diagnose und Therapie der chronischen Herzinsuffizienz betonen, wie wichtig es ist, die Mitralinsuffizienz erst nach mehreren Monaten stabiler und maximal verträglicher pharmakologischer Therapie neu zu bewerten [10]. Die Wiederholungsuntersuchung sollte immer in einem kardial kompensierten Zustand (optimaler Volumenstatus) des Patienten durchgeführt werden.
Wenn die Mitralinsuffizienz immer noch mäßig bis schwer ist, insbesondere bei der Behandlung von Hochrisikopatienten, sollten die Behandlungsoptionen (chirurgische oder Transkatheter-Klappenreparatur) in einem Herzteam aus Kardiologen, Herzchirurgen und Spezialisten für Bildgebung evaluiert werden [9]. Die Bewertung sollte eine Risikostratifizierung nach Symptomen (im Zusammenhang mit der Klappenerkrankung), begleitendem Vorhofflimmern, Alter, relevanten Komorbiditäten, linksventrikulärer Funktion, PH, Notwendigkeit eines begleitenden chirurgischen Eingriffs (d.h. Revaskularisierung) und der Eignung der Klappenreparatur umfassen, die die wichtigsten Prädiktoren für das postoperative Ergebnis sind [10]. Die operative Sterblichkeit kann mit verschiedenen Scoring-Systemen, z.B. STS oder EuroSCORE II, eingeschätzt werden. Dazu gehören insbesondere Indizes zur Bewertung der funktionellen und kognitiven Fähigkeiten und der Gebrechlichkeit bei älteren Menschen. Die endgültige Entscheidung für die optimale Behandlungsoption sollte gemeinsam mit dem Patienten und seiner Familie getroffen werden.
Mitraclip-Therapie
Die Mitraclip-Therapie wurde erfolgreich zur Behandlung der funktionellen oder degenerativen Mitralinsuffizienz eingesetzt. Der Mitraclip wurde in der multizentrischen, randomisierten, kontrollierten Studie EVEREST untersucht, an der nur operierbare Patienten teilnahmen [11]. Die Mehrheit der in EVEREST aufgenommenen Patienten hatte eine degenerative, aber jeder vierte Patient hatte eine funktionelle Mitralinsuffizienz. In diesem Zusammenhang sind die Ergebnisse von ACCESS-EU, einer prospektiven, multizentrischen, nicht-randomisierten Studie in Europa, von Bedeutung, die vor allem Hochrisiko-Patienten (NYHA III-IV und LVEF ≤40% in 85%; EuroSCORE: 23±18,3) einschließt, die vor allem eine funktionelle Ätiologie haben (n=393/510) [12]. Die Sterblichkeitsrate nach dreißig Tagen betrug 3,4% und die Schlaganfallrate 0,7%, wobei es keine Fälle von intraprozeduralen Todesfällen oder Clip-Embolisationen gab.
Zusammenfassung
Zusammenfassend lässt sich sagen, dass die PH ein wichtiges Anzeichen für eine fortgeschrittene LHD mit schlechterem Ausgang ist. Der wichtigste therapeutische Ansatz sollte nach einer sorgfältigen Untersuchung auf den Ursprung der LHD gerichtet sein. In sehr ausgewählten Fällen könnte eine für PAH zugelassene Therapie, d.h. PDE5i, als Überbrückung bis zur Herztransplantation und nach einem linksventrikulären Unterstützungssystem bei schwer eingeschränkter rechtsventrikulärer Funktion angezeigt sein. Da es immer noch an Beweisen für die Wirksamkeit aus groß angelegten, langfristigen placebokontrollierten Studien mangelt, wird von der Verwendung von PAH-Medikamenten bei anderen Formen der PH außerhalb von Expertenzentren abgeraten.
Referenzliste:
- Vachiery JL, et al: Pulmonale Hypertonie aufgrund von Linksherzerkrankungen. J Am Coll Cardiol 2013; 62(25 Suppl): D100-108.
- Galie N, et al: Leitlinien für die Diagnose und Behandlung der pulmonalen Hypertonie. Die Task Force für die Diagnose und Behandlung der pulmonalen Hypertonie der Europäischen Gesellschaft für Kardiologie (ESC) und der European Respiratory Society (ERS). Eur Heart J 2009; 30(20): 2493-2537.
- Galie N, et al.: 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Die Gemeinsame Task Force für die Diagnose und Behandlung der pulmonalen Hypertonie der Europäischen Gesellschaft für Kardiologie (ESC) und der European Respiratory Society (ERS). Eur Heart J 2016; 37(1): 67-119.
- Ghio S, et al: Unabhängiger und additiver prognostischer Wert der systolischen Funktion des rechten Ventrikels und des Drucks in der Lungenarterie bei Patienten mit chronischer Herzinsuffizienz. J Am Coll Cardiol 2001; 37(1): 183-188.
- Lewis GD, et al: Sildenafil verbessert die körperliche Leistungsfähigkeit und die Lebensqualität von Patienten mit systolischer Herzinsuffizienz und sekundärer pulmonaler Hypertonie. Circulation 2007; 116(14): 1555-1562.
- Shan X, et al: Unterschiedliche Expression von PDE5 in versagendem und nicht versagendem menschlichem Myokard. Circ Heart Fail 2012; 5(1): 79-86.
- Mehra MR, et al: Aufnahmekriterien für die Herztransplantation: Richtlinien der Internationalen Gesellschaft für Herz- und Lungentransplantation für die Betreuung von Herztransplantationskandidaten–2006. J Heart Lung Transplant 2006; 25(9): 1024-1042.
- Feldman D, et al: Die Leitlinien 2013 der Internationalen Gesellschaft für Herz- und Lungentransplantation zur mechanischen Kreislaufunterstützung. Executive summary. J Heart Lung Transplant 2013; 32(2): 157-187.
- Vahanian A, et al: Leitlinien für die Behandlung von Herzklappenerkrankungen (Version 2012). Die Gemeinsame Task Force zur Behandlung von Herzklappenerkrankungen der Europäischen Gesellschaft für Kardiologie (ESC) und der Europäischen Vereinigung für Herz- und Thoraxchirurgie (EACTS). Eur J Cardiothorac Surg 2012; 42(4): S1-44.
- McMurray JJ, et al: ESC-Leitlinien für die Diagnose und Behandlung von akuter und chronischer Herzinsuffizienz 2012. Die Task Force für die Diagnose und Behandlung der akuten und chronischen Herzinsuffizienz 2012 der Europäischen Gesellschaft für Kardiologie. Eur J Heart Fail 2012; 14(8): 803-869.
- Feldman T, et al: Perkutane Mitralreparatur mit dem MitraClip-System. Sicherheit und mittelfristige Haltbarkeit in der ersten EVEREST-Kohorte (Endovascular Valve Edge-to-Edge REpair Study). J Am Coll Cardiol 2009; 54(8): 686-694.
- Maisano F, et al.: Perkutane Mitralklappeninterventionen in der realen Welt. Früh- und 1-Jahres-Ergebnisse der ACCESS-EU, einer prospektiven, multizentrischen, nicht-randomisierten Studie nach der Zulassung der MitraClip-Therapie in Europa. J Am Coll Cardiol 2013; 62(12): 1052-1061.
CARDIOVASC 2016; 15(2): 11-15