Welche Studienphasen durchläuft ein neuer Wirkstoff, bis er in die klinische Praxis gelangt? Welche Unterschiede gibt es bei den Designs klinischer Studien? Welche Aspekte sind wichtig, um Ergebnisse interpretieren zu können? In diesem CME-Fortbildungsbeitrag wird die Entwicklung klinischer Studiendesigns bei chronisch-entzündlichen Darmerkrankungen (IBD) aufgezeigt und ausgeführt, wie sich Endpunkte von klinischen Messungen hin zu patientenbasierten Angaben verändern sowie sich gemischte Endpunkte aus endoskopischen sowie patientenbasierten Bewertungen zusammensetzen.
Partner
Autoren
- PD Dr. med. Pascal Juillerat
Publikation
- GASTROENTEROLOGIE PRAXIS
Related Topics
Dir könnte auch gefallen
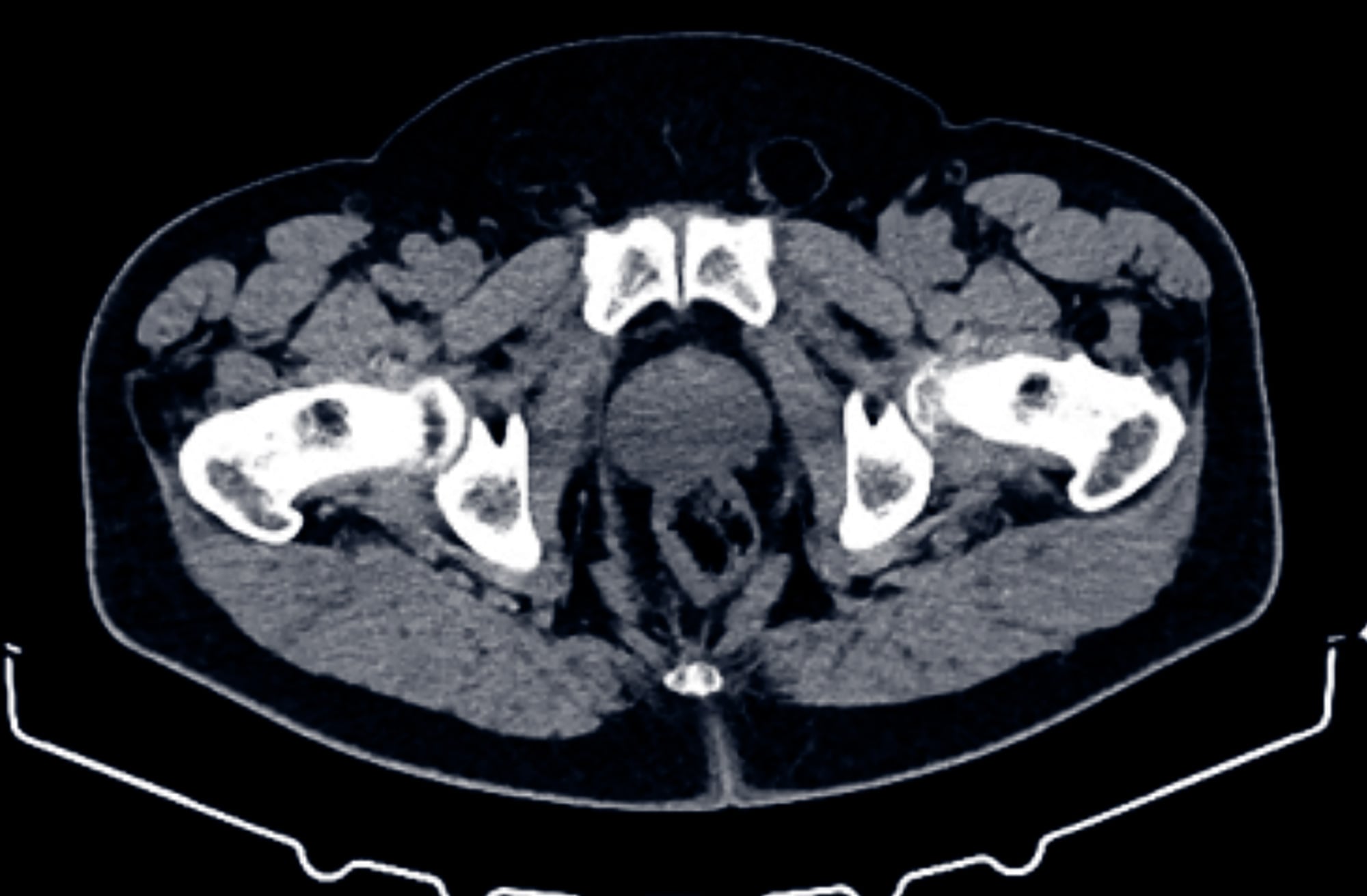
- Vom Symptom zur Diagnose
Abdominalschmerz – Prostatalipom
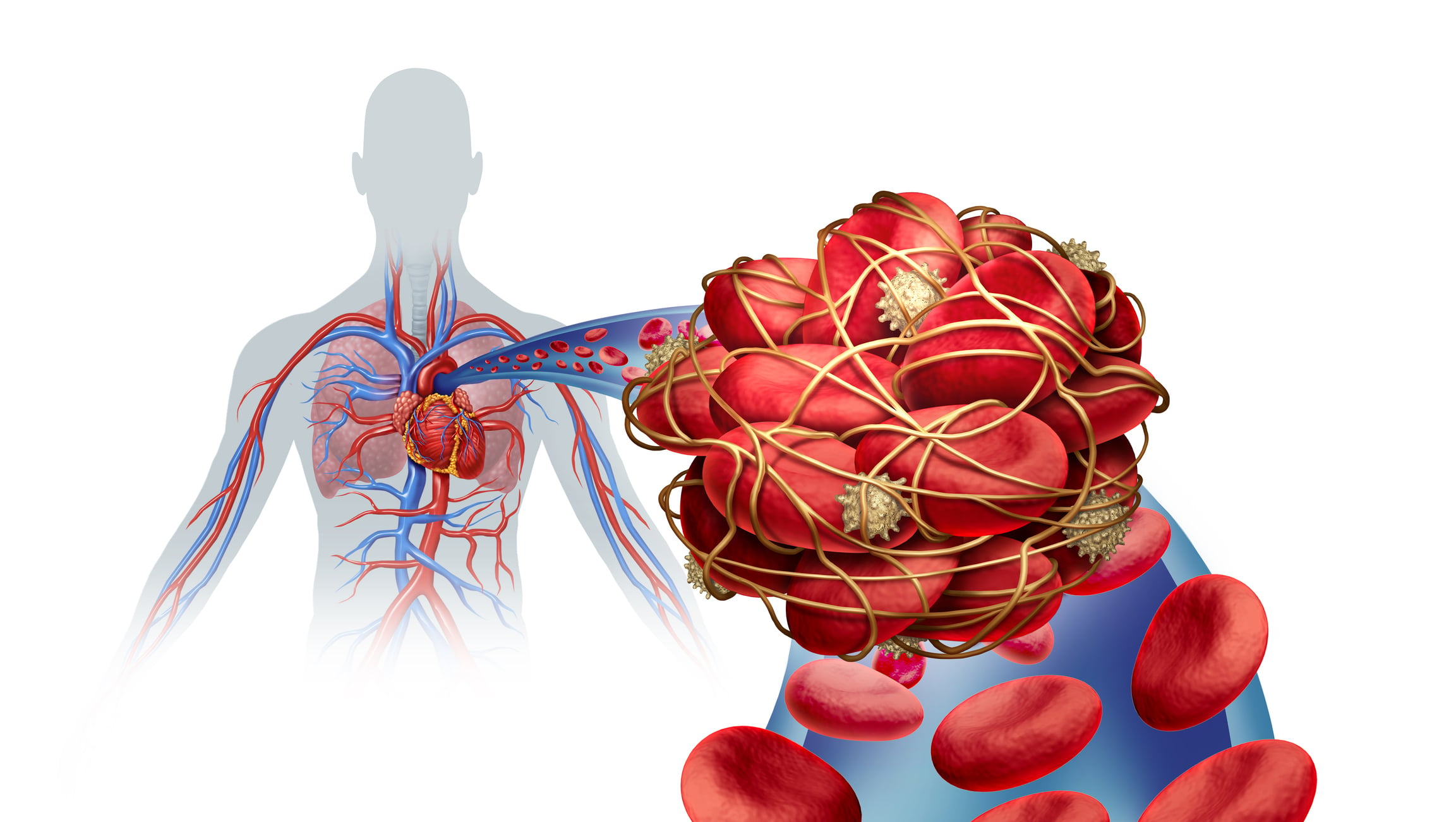
- Akute Lungenembolie: neue AHA/ACC-Leitlinie
Praxisrelevante Empfehlungen für risikostratifizierte Triage
- Warum Lipoprotein(a) das grösste therapeutische Vakuum der Kardiologie ist
Lp(a): Der unterschätzte Risikofaktor vor dem Wendepunkt
- Moderne Systemtherapeutika bei Hidradenitis suppurativa
Immunologische Fehlregulation im Visier etlicher Biologika und «Small molecules»
- Perimenopausale Depression, PMDS und Tokophobie
Psychosomatik und mentale Gesundheit in der Gynäkologie
- Proteine in der Wundheilung
Führen spezielle Aminosäuren zum Erfolg?
- Plastische Chirurgie und Rekonstruktive Mikrochirurgie beim DFS
Funktioneller Extremitätenerhalt zwischen Infektkontrolle, Gefässmedizin und Resurfacing
- Polyzystisches Ovarsyndrom 2025/2026